- 分類:標靶治療
- 作者 陳駿逸醫師
- 點擊數:57554
Her2陰性高惡性轉移性乳癌
( 五) 新名詞:HER2陰性高惡性轉移性乳癌
於是乎就有些極具眼光的臨床醫師,希望能夠藉由疾病的臨床特性與乳癌本身的生物特徵之相關資訊,界定出何人屬於預後甚差的乳癌族群。這群惡性度較高的乳癌族群,通常是高復發風險、病情進展較快,處理起來頗為棘手、存活率甚差、死亡率甚高的乳癌族群。目前迫切需要找出這群”最難搞”、”騎重機”的HER2陰性轉移性乳癌,然後找出最適合此一族群且最有效的個體化精準醫療。
目前個體化的精準醫療,往往採取”同病異治”的做法,頗有類似華佗之所以被稱為神醫的精隨。怎麼這樣說呢?
話說當年府中官吏倪尋、李延同時來找華佗就診,兩人都是頭痛發燒,病痛,而且癥狀完全相同。華佗卻說:”倪尋應該把病邪瀉下來,李延應當發汗驅病。”有人對這兩種不同療法提出疑問。於是華佗回答說:倪尋是外實症,而李延是內實症,所以治療他們也應當用不同的方法。’馬上分別給兩人服藥,第二天一大早兩人一同病好起床了。
對於乳癌患者,分析病人、疾病的臨床特性與本身乳癌的生物特徵相關資訊,將病患有效地分類,然後給予最適合且最有效的個體化精準醫療。這就是當年華陀同病異治理念的極致衍生,所以如何找出HER2陰性高惡性轉移性乳癌的特定族群,是解決”難搞”乳癌、”騎重機”乳癌的第一步。
(1) 魔鬼總是藏在細節裡
Arpino 教授希望從2012年至2014年的醫學資料庫Pubmed中,找到Her2陰性高惡性轉移性乳癌所具備充分實證等級的潛在預後危險因子,分別從病人、疾病的臨床特性與乳癌生物特徵之相關資訊介入,結果最後找到影響Her2陰性高惡性轉移性乳癌存活的六大危險因子,而且這六者都屬於臨床上證據等級最高的。如下列所示:
| Her2陰性高惡性轉移性乳癌的六大危險因子 |
| 1.存在有內臟器官轉移(visceral metastases) |
| 2.轉移器官數 (number of metastatic sites) 3個以上 |
| 3.無病間期(手術後至轉移復發的間隔期) (disease-free interval ) 少於2年 |
| 4.循環腫瘤細胞數量( presence of CTCs)≧5 per 7.5 ml |
| 5.三陰性 (triple-negative disease)乳癌 |
| 6.腫瘤細胞分化級數( tumor grade ):高度惡性 |
根據其分析資料指出,具有充分實證研究發現的患者出現肝、肺轉移或大於三處器官轉移者,其死亡風險提高了2.47倍!另外,無病間期(手術後至轉移復發的間隔期) 少於2年者相較於無病間期大於或等於2年者,死亡風險提高了2.7倍!
台灣也有類似的資料,林口長庚醫院乳癌團隊為了辨識哪些危險因子可用來預測乳癌病情發展,特別將12年的時間(西元2000-2012年)收治的1763名轉移性乳癌患者,其中1224位有癌症遠端轉移者的臨床診治資料,分析其存活情況;並進一步分析Her2陰性高惡性乳癌的危險因子,預測其轉移後2年內死亡風險。
林口長庚醫院乳癌團隊的研究結果,發現包括轉移至腦、肝、肺而有明顯病徵;轉移部位超過3處、術後2年內即復發,以及年齡大於70歲、三陰性乳癌等,都是影響乳癌患者預後及存活的重要危險因子。基本上,林口長庚醫院對於高惡性晚期乳癌的預後因子的分析,與分析較為廣泛且嚴謹的Arpino 教授發表於知名國際期刊” Breast”的研究發現,頗有”英雄所見略同”之感,大體上也是以有內臟器官轉移、3個以上的轉移器官數、無病間期(手術後至轉移復發的間隔期)少於2年、三陰性乳癌等為主要危險因子,然而有越多的危險因子存在,其Her2陰性高惡性轉移性乳癌的預後也越差。
中山醫學大學附設醫院乳房及內分泌外科姚忠瑾醫師也曾經提到,乳癌的發展,有的腫瘤像彩椒,雖然大顆,但不嗆辣;有的則像朝天椒,體積雖小,卻辣得讓人噴淚。這類Her2陰性高惡性乳癌就像朝天椒,小小一顆,即使早期發現,但因為這類腫瘤發展快速,一下子就轉移,復發的機會較高,三陰性亡死亡率也較高。
(2) Her2陰性高惡性轉移性乳癌治療的窘境
當我們已經釐清如何界定Her2陰性高惡性轉移性乳癌的定義,以及如何藉由危險因子的多寡,對Her2陰性高惡性轉移性乳癌的預後進行評估,接下來就是擬定針對Her2陰性高惡性轉移性乳癌的有效戰略。
目前醫學界對於轉移性乳癌的治療目標,控制腫瘤體積、緩解腫瘤症狀以及延長疾病無惡化存活時間為首要目標,如此才有機會提供病人達到最佳生活品質的次要目標,長期的目標則延長病患整體存活時間。傳統上對於高惡性轉移性乳癌的最佳策略,說穿了只有全身性化療,姑且不論全身性化療的毒性與耐受性如何,如果討論其Her2陰性高惡性轉移性乳癌的化療成績,可能要令許多專業人士大吐苦水,第一線化療的疾病控制時間,單一藥物的化療往往只有4-6個月的疾病控制時間,而合併兩種以上的化療藥物治療也只有6-8個月;至於第一線化療的有效反應率,則不超過25%。
對付這群難搞、病情進展迅速、腫瘤範圍較大的Her2陰性高惡性轉移性乳癌,傳統第一線治療的化療,看來不只是不足,而且是極為危險的治療方式,單獨化療對於病情的控制不佳,連對付轉移性乳癌的控制腫瘤體積、緩解腫瘤症狀以及延長疾病無惡化存活時間的首要目標,都表現得”二二六六”、不盡理想,如此更遑論達到病人最佳生活品質的次要目標,以及延長病患整體的存活時期的長期目標。
(3) 翻轉Her2陰性高惡性轉移性乳癌的治療成績
對於這樣的困境,我們真的只能坐視嗎?還是可以有機會來拚個翻轉呢?
到目前為止,化療仍然是這群Her2陰性高惡性轉移性乳癌的最佳策略,而想要改變全身性化療病情控制不佳的窘境,可以先從改善腫瘤體積的控制、腫瘤症狀的緩解著手,如此可以水到渠成地延長疾病無惡化的存活時間。這樣的思維確實合理,然而可行嗎?
當癌細胞增生到一個階段的時候,會啟動腫瘤血管新生(Angiogenesis)的機制,讓腫瘤周遭正常的血管增生至腫瘤處,腫瘤會因此獲得從血管而來的大量養分、氧氣的補給,也讓腫瘤因為血管幹道的導入,幫助其進行血行性的轉移。然而,腫瘤本身及其周遭的血管,結構、特性都大異於正常的血管,且血管管壁並不完整,反而是管壁上有許多裂縫與破洞,無形間造成腫瘤血管通透性增加,也因此造成大量組織液從腫瘤血管破損的管壁滲出到腫塊內,造成腫瘤內間質壓力的提高,導致腫瘤更形缺氧、癌細胞內環境更偏酸性,如此反而會壓制了腫瘤周遭微環境的抗癌免疫細胞,造成腫瘤所在處局部免疫功能的顯著下降。
再者,腫瘤血管管壁裂縫與破洞頻繁的情形,也會使得原本要從血管運送至腫瘤處撲殺癌細胞的化療藥物,在運送過程中就被迫從血管管壁大量流失,造成最後至癌細胞的有效化療濃度大打折扣,導致化療”CP值”驟降,成為相對無效的化療。然而已經有許多學者發現,上述這些情形高度存在於三陰性的乳癌, 甚至更廣泛存在於高惡性轉移性乳癌。也正因為這些特性,讓高惡性轉移性乳癌病情進展快速、臨床處理起來頗為棘手,第一線全身性化療的有效反應率不超過25%,存活率甚差。
(4) 解鈴還須繫鈴人
看來想要翻轉Her2陰性高惡性轉移性乳癌臨床治療困境,可能要從改變腫瘤血管做起,讓腫瘤血管異乎正常血管的特性,來個撥亂反正,讓其正常化。既然一切都是腫瘤血管新生(Angiogenesis)機制啟動所造成的,何嘗不讓我們來個反轉,抑制腫瘤血管新生?
而抑制腫瘤血管新生的首推方法,就是應用抑制腫瘤血管新生的標靶藥物,現成已經可以用於乳癌的抑制腫瘤血管新生之標靶藥物,首選就是癌思停(bevacizumab, Avastin)。
癌思停也真的不失所望,在臨床前期的大量研究發現,癌思停確實能夠讓腫瘤血管正常化,改變腫瘤血管通透性,降地腫瘤內的間質壓力,如此便可以提高至癌細胞的有效化療濃度,增加原本化療的有效率;再者,也因為腫瘤血管正常化,使得腫瘤內的血液灌流增加,改善癌細胞內環境缺氧與偏酸性的環境,如此會刺激腫瘤周遭微環境的抗癌免疫細胞,造成腫瘤所在處局部免疫功能的顯著加強,減少癌細胞使壞的本錢。
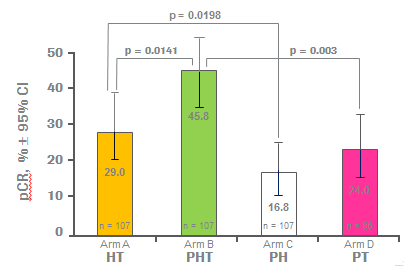
癌思停的基礎研究累積資訊,對我們臨床上處理Her2陰性之高惡性轉移性乳癌,想要改善全身性化療的有效率,改善腫瘤體積的控制與腫瘤症狀的緩解,進而比單獨化療更能夠延長疾病無惡化的存活期,似乎提供了一線曙光。針對Her2陰性高惡性轉移性乳癌,於傳統治療策略之化學治療基礎上,再加上癌思停,或許有可能讓Her2陰性高惡性轉移性乳癌目前僅有化療一途、且是第一線治療的頹勢,有機會拚翻轉。
