- 分類:癌症治療新知
- 作者 癌症新觀點/話聊俱樂部 陳駿逸醫師
- 點擊數:1122
2022年陳駿逸醫師談關於胰臟癌標靶與免疫治療的新思維
第 2 頁,共 3 頁
針對胰臟癌最常見的KRA S基因突變,如何進行反擊呢?
超過90%的胰臟癌出現致癌性基因KRA的S突變,但基因出現特定突變位點的發生率是有所不同,包括G12D(占比41%)、G12V(占比34%)、G12R(占比16%)、Q61H(占比4%)和G12 C(占比少於1%)。不同突變位點的KRAS基因在胰臟癌中會有不同的致癌特性。例如:在手術可切除的胰臟癌中,屬於KRAS G12D突變的預後,則是比所有其他魏點的KRAS突變和野生型KRAS之胰臟癌,都要來得更差。
儘管胰臟癌中有KRAS突變的頻率如此地高,但由於突變RAS蛋白缺乏適合高親和力結合的藥物口袋,讓科學家開發RAS標靶藥物遇到重重難關。
隨著特異性KRAS突變之標靶治療藥物研發的進展,首個特異性針對KRAS G12C的小分子標靶藥物ARS-1620,在胰臟癌的體外和體內模型中展示出抗腫瘤的療效。後續,KRAS G12C之標靶治療藥物更是青出於藍,而更勝於藍,舉凡sotorasib、adagrasib等都對轉移性胰臟癌的患者表現出臨床療效。
目前,相關研究正在進行更新、更好的KRAS G12D標靶藥物的研發與評估。而除了KRAS等位基因的選擇性小分子標靶藥物外,新型的、臨床等級的泛RAS抑制劑RMC-6236也可以讓KRAS突變的腫瘤體積減小;選擇性口服小分子SOS1抑制劑BI-3406在KRAS驅動的癌症模型中,展示出具有顯著降低腫瘤生長和GTP–RAS的水準。另一種突變型KRAS胰臟癌的治療方法,使用與脂質納米顆粒包裹的mRNA疫苗策略。
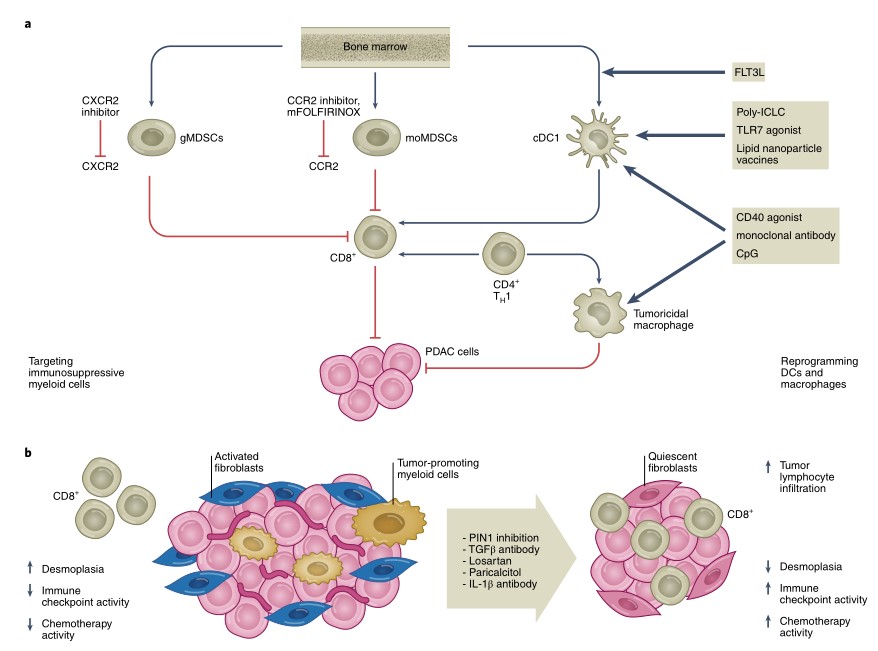
KRAS突變型與野生型胰臟癌治療的前景
