- 分類:免疫治療
- 作者 陳駿逸
- 點擊數:976
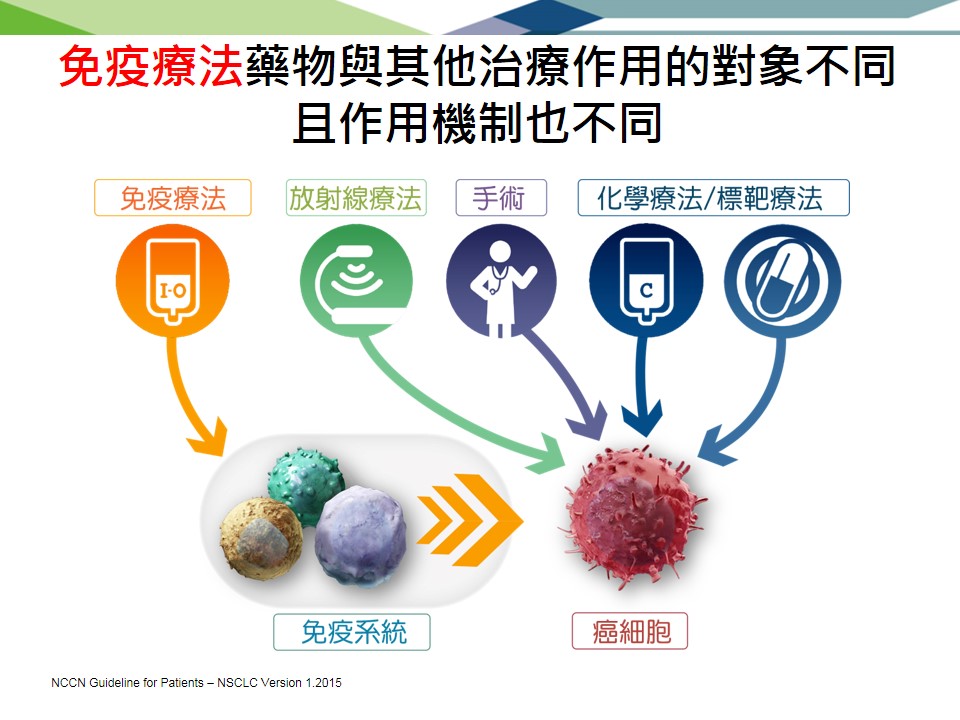
從2018年度諾貝爾生理醫學獎 談肺癌免疫治療的新進展
2018年度諾貝爾獎名單今日起陸續揭曉,率先公布的是生理醫學獎,美日兩名免疫學者因研究癌症治療一同獲獎。得主是美國德州德州大學安德森癌症中心的艾利森(James P. Allison )和日本京都大學的本庶佑,原因是「抑制抑制免疫調節的癌症治療方式。諾貝爾委員會形容,兩人的成就是人類對抗癌症的重要里程碑,他們「鬆開免疫細胞的煞車」,利用免疫系統的能力來攻擊癌症細胞。

今年70歲的艾利森研究免疫系統內,一種可以用作「煞車」(停止)機制的蛋白。艾利森發現,透過釋放體內的「煞車」機制,或可以促進免疫細胞攻擊癌細胞,他更將這個概念,發展成治療癌症病人的新方法。76歲的本庶佑則在研究中,發現在免疫細胞中有一種蛋白,同樣可以有「煞停」作用,但其運作基制與艾利森的發現不同。研究人員其後透過本庶佑的研究成果,發展出新的治癌療法,並已獲證明十分有效。
諾貝爾委員會已通知本庶佑,此刻在日本京都大學的他表示非常高興,並誓言要持續研究癌症治療,救更多的病患,「我希望繼續研究......讓這種免疫治療拯救更多病患。」至於在美國德州的艾利森,可能因為時差關係,暫時沒有消息。
兩位學者的免疫研究在國際早有聲譽,曾雙雙獲得台灣的「唐獎」榮譽。本屆得獎者可獲900萬瑞典克朗(約3090萬元台幣)獎金,金額與上屆相同。
在這個背景下,目前看來,在整個肺癌的治療上,包括第一線、二線和三線治療,免疫治療已經佔據了“半壁江山”,但單獨使用免疫治療總體有效率並不高,除了何杰金氏淋巴瘤外,整個實體瘤包括肺癌的有效率約20%~30%。
在這樣的情況下,臨床醫師有兩條思路來解決這個困境:
1)尋找預測療效的生物標記物,從而選擇出對免疫治療有效的患者,鑑別出無效的患者,同時,避免選出副作用大的患者;
2)免疫聯合其他治療,包括聯合有效的化療、抗血管新生治療或標靶治療。
關於尋找預測療效的生物標記物:
具有預測療效效果的生物標誌物可以讓們找到有效的人群。
PD-L1是目前唯一被公認是免疫治療的相對可靠的檢測標誌物。
KEYNOTE-024研究告訴我們,PD-L1≥50%的患者可以明顯從pembrolizumab藥治療中獲得總生存期提高的意義;在KEYNOTE-189研究中,pembrolizumab+ pemetrexed和鉑類化療藥物後,即便是PD-L1陰性或低表達水平的患者也有生存獲益,雖然PD-L1≥50%的亞組與PD-L1在1%~49%的亞組患者相比,免疫聯合化療帶來更顯著的生存獲益。因此,對於PD-L1≥50%的患者,免疫聯合化學治療,效果似乎更佳,臨床上是選擇免疫單一藥要,還是聯合免疫與化療治療,值得大家思考。
PD-L1檢測目前有”洋蔥”
PD-L1並不是沒有缺點,最大的缺點是PD-L1存在相當程度的異質性。2018年有研究指出從90度進針或從180度進針獲取腫瘤標本,而後進行PD-L1檢測,兩個結果竟然完全相反,一個角度進針標本的PD-L1表達50%以上為陽性,另一個角度標本檢測呈陰性。臨床上,不可能做360度穿刺以獲取一個患者的組織標本。另外,即便是用不同抗體檢測,PD-L1仍然是陰性,還是有16%患者受惠於免疫治療。
另一生物標記物TMB檢測,仍有待繼續研究
腫瘤突變負荷量(TMB)的檢測仍存在很大的問題。CHECKMATE-026研究乃是探討非小細胞肺癌患者使用nivolumab對比標準化療作為第一線藥物治療研究,因為收入了較多PD-L1表達弱陽性的患者,導致了研究結果沒有呈現正面意義。但是最終次分析顯示,即使最初將PD—L1的閥值(cutoff)設置為50%,CHECKMATE-026的研究依然會是陰性結果。接著nivolumab繼續去探索是否有新的生物標記物,可以用來篩選nivolumab適用的族群,他們找到了TMB。在CHECKMATE-026的後續性分析中,發現TMB>10突變/Mb的患者接受nivolumab治療後,預後明顯優於化療組,而TMB低的患者還不如接受化療。
CHECKMATE-026研究顯示,TMB確實是可以很好的預測疾病有效控制時間(PFS),但是對整體存活率(OS)的預測,一直是兩條曲線拉不開,也就是說TMB在抗原的特異性暴露性方面具有優勢,好像告知我們該患者屬於一個特定的基因型態,可以預測好的療效反應率,高TMB的非小細胞肺癌患者對免疫治療可產生快速反應,因為nivolumab治療後有效率(ORR)較高,但是長期的生存的獲益是否還可以依賴腫瘤新抗原激發的免疫反應來持續的維持尚未可知。CHECKMATE-227研究結果也是如此,高的TMB,可以預測很好的PFS,但卻不是好的OS預測。
另外, TMB平均檢測時間需要兩周以上,長時間的等待對於患者來說是一個很五味雜陳的過程。因此美國NCCN治療共識,目前的第一線治療考量選擇用何種治療時候,還是推薦PD-L1的檢測,後續才會選擇這個TMB,很大因素是考慮到了TMB的檢測時間過長這個問題。
還有沒有其他潛在的生物標記物呢?
DNA修復相關基因(DDR)或許有機會成免疫療效預測的生物標記物。
其它的生物標記物,比如MSI-H和dMMR。雖然當前已經明確了MSI-H和dMMR亞型的實體瘤患者是可以從免疫治療中獲益,但這部分患者的比例在肺癌患者中非常低,不足5%;而且,雖然針對MSI-H和dMMR的患者,免疫治療的有效率就會非常高,但是尚無法肯定對陰性的患者絕對無效。再者如Tony Mok教授近期發表關於MSI-H/dMMR,以及BRCA1和BRCA2、pole突變的研究結果(發表於Clinical Cancer Research)顯示,當多條DNA損傷修復(DDR)途徑發生突變時,例如:NHEJ、HR、BER突變,縱使TMB低,仍然有機會對免疫治療受益。免疫治療的預後比較好。
最初關於這方面的研究見於黑色素瘤的治療,BRCA2突變的患者TMB明顯增高,經過免疫治療的預後較好。之後,在大腸癌,DNA損傷修復基因(DDR)突變的患者預後也非常好。在泌尿系統腫瘤,如尿路上皮癌, DDR表現陽性患者的預後也非常好。DDR相關的基因如果是單一突變,突變負荷會有所增加,但如果是多個通路發生共突變,突變負荷增加應該會非常高,接近于dMMR的水準。如果在肺癌中進行驗證,將肺癌TMB低的患者用DDR共突變這個指標來區分,發現可以很好的區分預後,說明可以通過DDR的共同突變來預測療效。對於PD-L1陰性的患者也可以通過DDR的共突變來區分預後。所以未來DDR可能會是臨床具有療效效預測價值的一個生物標記物。
有無臨床預測性指標可以做為生物標記物呢
出現白斑症或是頭髮變烏黑,也是免疫治療的臨床預測性指標。
非小細胞肺癌T790M突變陽性的患者接受免疫治療的效果不好。1期臨床試驗資料顯示T790M突變陽性的非小細胞肺癌患者基本上對免疫治療是無效的,且毒性很大,出現7例間質性肺炎,該臨床試驗被終止。2018今年ASCO的真實世界資料顯示EGFR突變的非小細胞肺癌患者效果也不好,但並不是所有的突變患者效果都不好。CHECKMATE-037研究結果顯示,ALK重排陽性患者對免疫治療是無效的,還有一定程度的傷害性,研究中有5個肝毒性,2個死亡,對於這類患者,免疫治療不僅療效不好,而且毒性非常大。而IMpower 150的免疫聯合有效的化療、抗血管新生治療,似乎提供了一個解決的方向。但今年也有研究發現有20種非經典突變,對傳統的標靶治療效果不好,但免疫治療有可能效果會好。
陳駿逸醫師目前擔任癌症中醫與西醫臨床治療醫師,著有”擊退癌疲憊 醫師該告訴你的癌後養生術”(康健出版),專職中西醫結合癌症治療與癌友關懷之公益活動,同時熱心致力於正確癌症照護資訊之推廣與傳遞,其所創建之台中市全方位癌症關懷協會http://www.cancerinfotw.org,乃是專業照護人員、社會賢達貢獻所學,所建構的癌症診療與照護資訊平臺。
此處文章乃是醫療照護資訊的整理,請勿引據文章內容自行採取醫療決定;如有臨床治療之需求,建議還是應該尋求專業醫療人員的協助。如有任何謬誤或建議,懇請不吝指教。
想要閱覽作者撰寫的更多相關癌症資訊,歡迎前往陳駿逸醫師官網”話聊俱樂部” http://cancerfree.medicalmap.tw/。
想要瞭解作者的資訊也請至http://cancerfree.medicalmap.tw/點閱”陳駿逸醫師簡介”
