- 分類:陳駿逸醫師的話聊俱樂部
- 作者 台中市全方位癌症關懷協會
- 點擊數:3909
三陰性晚期乳癌有何治療的新選擇
中醫台院腫瘤中心/台中市全方位癌症關懷協會理事長
陳駿逸醫師主講
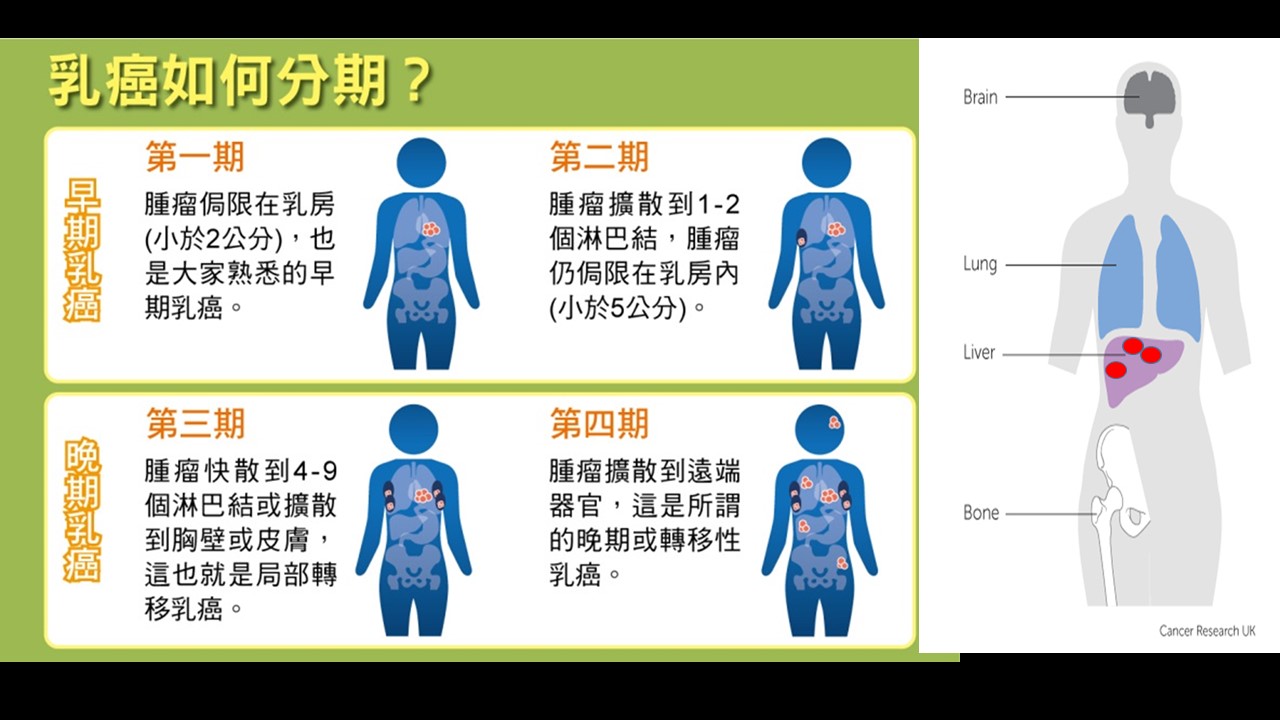
乳癌的分期:乳癌分期的主要目的在確立治療方式的選擇,評估預後及比較不同治療方式的結果。
目前乳癌的分期是依據腫瘤大小 (T)、腋下淋巴腺轉移與否 (N)、遠處是否轉移 (M) 等TNM系統來分為:(依據UICC,AJCC 1988分期)
1. 零期乳癌:即原位癌,為最早期乳癌,癌細胞仍在乳腺管基底層內。
2. 第一期乳癌:腫瘤小於兩公分以下的浸潤癌且腋下淋巴結無癌轉移。
3. 第二期乳癌:腫瘤在兩公分至五公分之間的浸潤癌;或腫瘤小於兩公分但腋下淋巴結有癌轉移。
4. 第三期乳癌:局部廣泛性乳癌,腫瘤大於五公分的浸潤癌且腋下淋巴結有任何癌轉移或有胸壁皮膚的浸潤乳癌。
5. 第四期乳癌:轉移性乳癌,已有遠處器官轉移 (如肝、肺、骨) 等。
乳癌分型:
1. 管腔A型 ER陽性/PR陽性/Her-2陰性/Ki67低
2. 管腔B型(Her-2陰性) B1 ER陽性/PR陽性/Her-2陰性/Ki67高
3. 管腔B型(Her-2陽性) B2 ER陽性/PR陽性/Her-2陽性
4. Her-2陽性型 ER陰性/PR陰性/Her-2陽性
5. 三陰性型 ER陰性/PR陰性/Her-2陰性
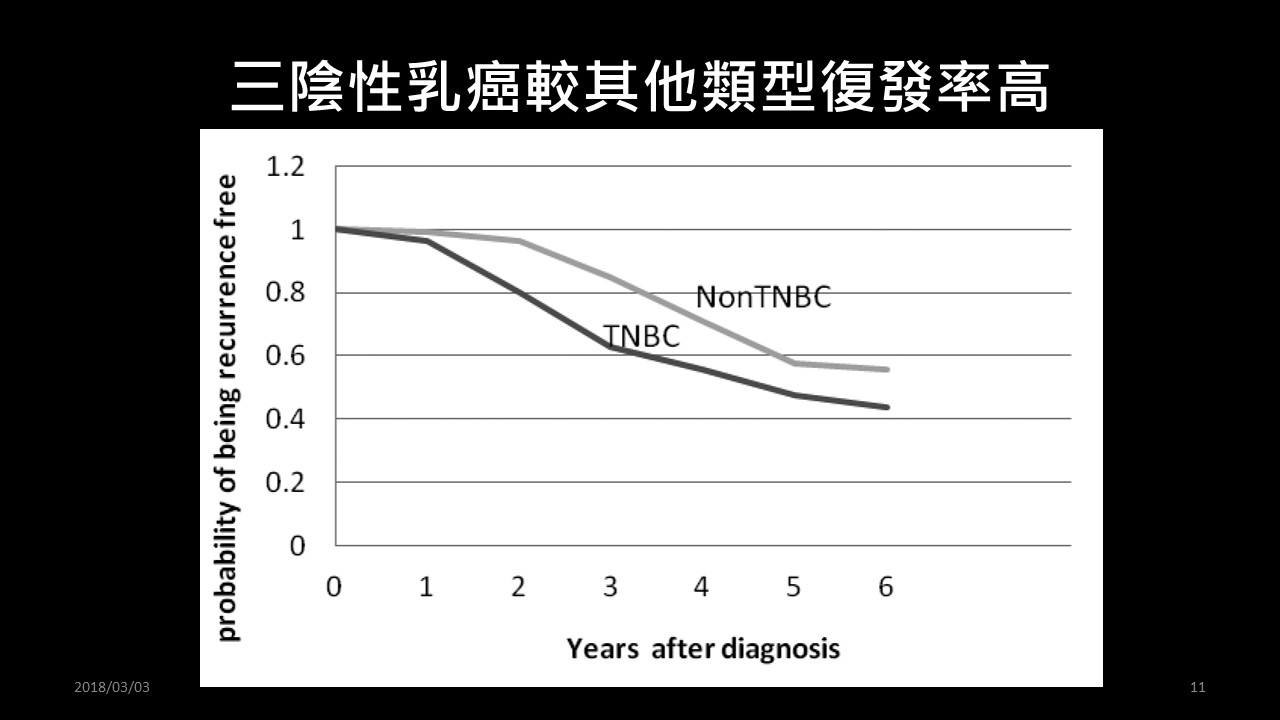
三陰性乳癌較其他類型復發率高,在復發分佈時間點上,前三年 ( 尤其 1-2 年 ) 是三陰性乳癌復發最常見的高峰期,但到了 7-8 年後三陰性乳癌的復發比率反而比非三陰性乳癌來的低。
目前第4期三陰性乳癌標準: 全身性治療
合乎健保規定的癌友,2020年11月開始健保會給付三陰性乳癌患者使用標靶藥物PARP抑制劑-olaparibDNA破損後會啟動修復機制,PARP是參與許多細胞過程如DNA修復,基因組穩定性,和程序性細胞死亡的蛋白質家族,BRCA1/2是這一群修復蛋白團隊的重要成員三陰性乳癌約佔乳癌中15-20%,其 中 10-20% 帶有生殖細胞BRCA1/2 致病性或疑似致病性的基因突變,反之乳癌與遺傳基因相關約佔5-10%,具有生殖細胞BRCA1/2 致病性或疑似致病性的基因突變的乳癌有90% 是三陰性乳癌( 尤其 BRCA1 ) 。
關於三陰性乳癌標靶藥物PARP抑制劑-olaparib 目前即將給付 ( 最後請參考健保署的網站公布資訊 ) :申請藥物使用時候,必須符合下列條件:
1.三陰性乳癌病人,也就是病理切片報告上的荷爾蒙接受體(ER與PR)及 HER2 受體皆為陰性的乳癌,而且是轉移性乳癌,亦即是第四期乳癌,指的是有遠端器官或淋巴接轉移的乳癌。
2. olaparib只被核准單獨使用PARP抑制劑-olaparib。目前實證醫學也不建議PARP抑制劑聯合化療使用。
3. 關於有需要使用過化療的規定:也就是先前可能是1-3期三陰性乳癌病人,且1-3期期間有使用過前導性、術後輔助性化療的療程與醫療紀錄,但後來不幸復發轉移成第四期乳癌,則可以在第四期乳癌優先於第一線治療就可以向健保署提出專案申請olaparib。但是如果一開始確診為第四期三陰性乳癌的病人,就需要先接受過專為轉移性乳癌的化療後,之後才可以向健保署提出專案申請olaparib。
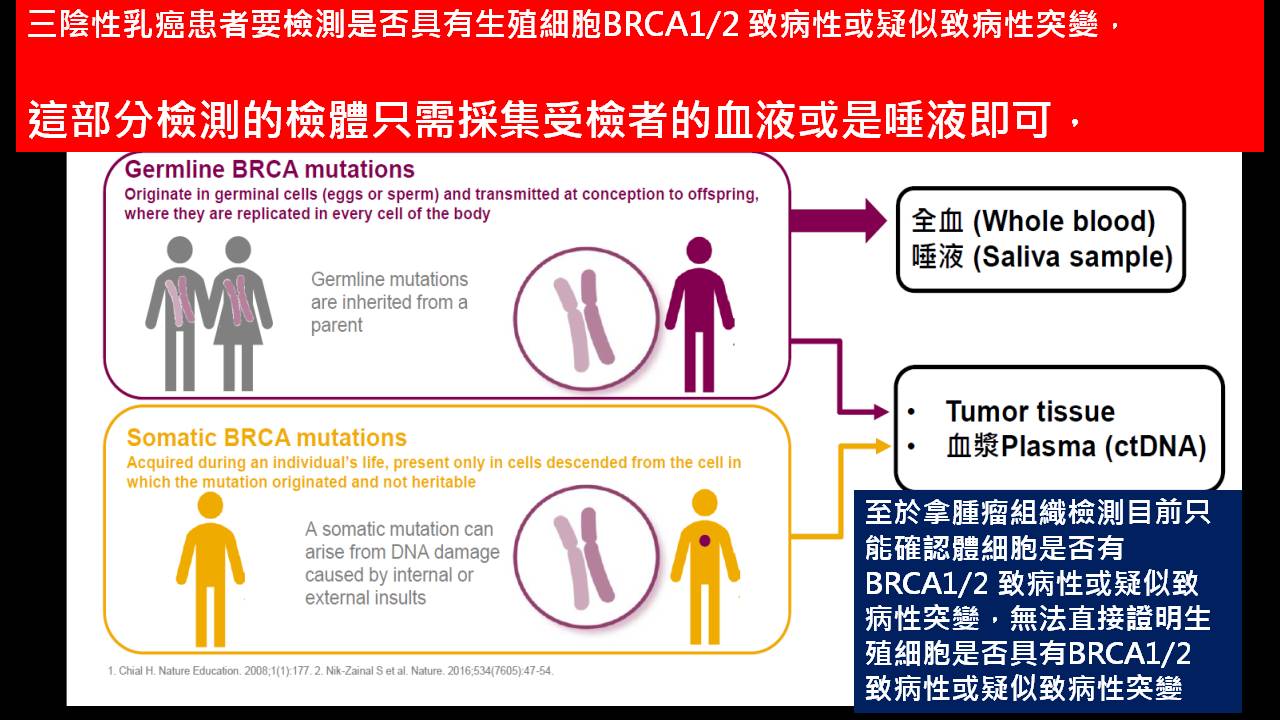
4.最後也是最重要的給付條件,那就是具備生殖細胞BRCA1/2 致病性或疑似致病性突變之三陰性乳癌。並不是所有的三陰性乳癌患者都具有生殖細胞BRCA1/2 致病性或疑似致病性突變,而且向健保署提出專案申請olaparib時候,一定需要證明自己本身具有生殖細胞BRCA1/2 致病性或疑似致病性突變,方可有機會核准使用。
由於基因檢測費用目前可能健保未給付,而且目前台灣對於基因檢測的認證制度尚在進行中,選擇正確有公信力的檢測,檢測應交由經驗豐富、具有認證的實驗室來判定病人的基因突變狀態。 要選擇基因檢測的平台要審慎評估,因為BRCA1/2屬於相當大的基因片段,建議一定要用NGS及MLPA技術皆有的檢測平台,而且不是有所有突變的基因都是致病性或疑似致病性的突變,判定是否是致病性或疑似致病性的突變,需要強大的生物訊息分析團隊與資料庫,目前為止,台灣這兩方面的水平可以說是高度參差不齊,癌友一定要小心再小心。如果未能正確找出適合該藥物的病友,不只會延誤治療契機、破壞健保照顧癌友的美意,由裘莉事件來看,更會讓周遭親人失去提早預防癌症的契機;如果有偽陽性發生,很可能會浪費醫療資源或是延誤治療契機。所以相關檢測問題,建議諮詢有開設基因檢測特別門診的醫療單位。
對於發生復發或轉移的三陰性乳癌會考慮使用鉑金類,如:Carboplatin 或 順鉑 (Cisplatin)。紫杉醇類化療 Eribulin
第4期三陰性乳癌的第一線標準治療的選項之一免疫治療只能在衛福部特許之醫療場所執行
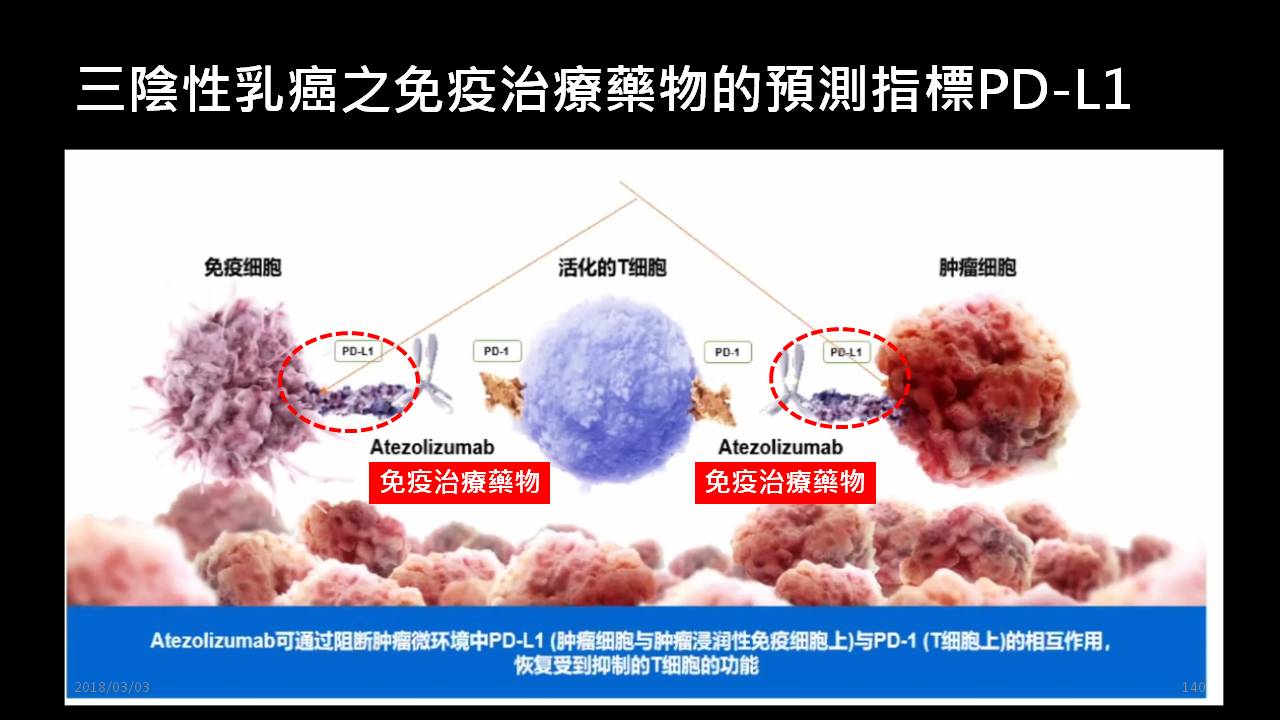
根據IMpassion 130研究的結果,提示Atezolizumab對於無法切除之局部晚期或轉移性三陰性乳癌患者帶來新的標準化之首波治療模式的新選項,可以讓疾病控制時間和整體存活時間獲得改善,特別是在PD-L1陽性患者中,才別具有臨床意義晚期三陰性乳癌之免疫治療藥物的預測指標,主要是看免疫細胞的PD-L1表達水平,PD-L1是要大於或等於1,才叫做陽性
如果SP142抗體檢測腫瘤免疫細胞的PD-L1表達水平呈現陰性者,目前並不建議首波全身性治療採用免疫聯合化療治療,因為如此做法似乎沒有比傳統治療模式要來得好。
免疫治療的生物標誌物PD-L1 絕對不是完美的,但卻是目前證據等級最高的免疫藥物預測指標
目前癌症免疫藥物雖然很多種,被美國及台灣FDA核准可用於治療無法切除之局部晚期或轉移性三陰性乳癌的免疫藥物就只有 Atezolizumab,其他藥物目前尚未受到官方核准或是研發失敗。單用免疫藥物atezolizumab,無法發揮有意義的抗腫瘤效果,一定要搭配化療。
日前公布的IMpassion131研究結果顯示:在PD-L1陽性族群中,與單獨太平洋紫杉醇組相比,免疫聯合化療組並沒有顯著降低患者癌症惡化和死亡的風險。此外,無論是在PD-L1陽性族群、還是在總體族群中,中期整體存活時間的分析結果都更支持免疫聯合化療組遜色於單獨太平洋紫杉醇。鑒于IMpassion131的研究未能達到預期的結果,美國FDA並沒有核准Atezolizumab 聯合太平洋紫杉醇在三陰性乳癌患者的使用。2020年9月8日,美國食品和藥物管理局(FDA)更向醫療健專業人員、腫瘤學臨床研究者和乳癌病人發出警示,認爲Atezolizumab 聯合太平洋紫杉醇的治療方案不適合用來治療三陰性乳癌患者。
經過改良,與白蛋白結合的新型紫杉醇製劑-白蛋白紫杉醇問世,nab-paclitaxel是一種無溶劑的紫杉醇製劑,目的除了能克服與溶劑有關的毒性,還能潛在地提高臨床療效。相對於原本的溶劑型紫杉醇,白蛋白紫杉醇的優勢在於它能夠向腫瘤細胞輸送更高劑量的紫杉醇,並降低嚴重毒性(包括嚴重的過敏反應)的發生率,且不需要類固醇的前置用藥。目前健保未給付免疫治療與白蛋白結合型紫杉醇,也就是因為免疫治療所費不貲,千萬別因為想要使用健保給付的化療藥物隊友,而功虧一簣、得不償失。
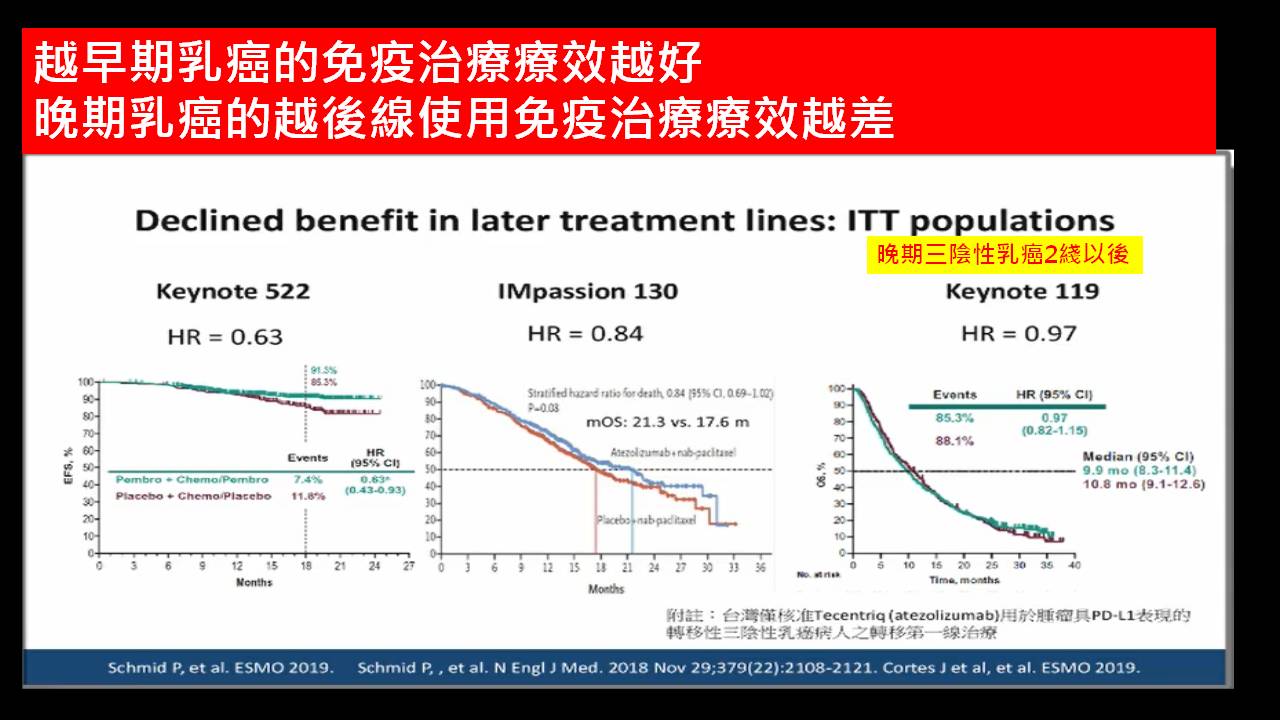
目前局部復發且無法切除之局部晚期三陰性乳癌,也必需在首波全身性治療就採用免疫聯合化學治療。而且如果拖到第二波、甚至第三波,或是無從選擇時再考慮使用免疫藥物治療,目前並不建議如此,主要是效果不彰。